Hüftendoprothetik
- die Implantation einer Hüftprothese gehört zu den chirurgischen Eingriffen, die zu der deutlichsten Verbesserung der Lebensqualität des Patienten führt (im Vergleich mit anderen Operationen)
- Indikation:
- Schmerzen und Funktionseinschränkung, die durch eine konservative Therapie allein nicht kontrolliert werden können
- Indikationsstellung nur gemeinsam mit dem Patienten
- seltener ist eine Operation aufgrund eines zunehmenden Knochenverlustes bzw. einer Deformität und einer Arrosion des lateralen Pfannerandes (Subluxation) oder des Pfannengrundes (Protrusio acetabuli) bereits bei geringeren Beschwerden indiziert
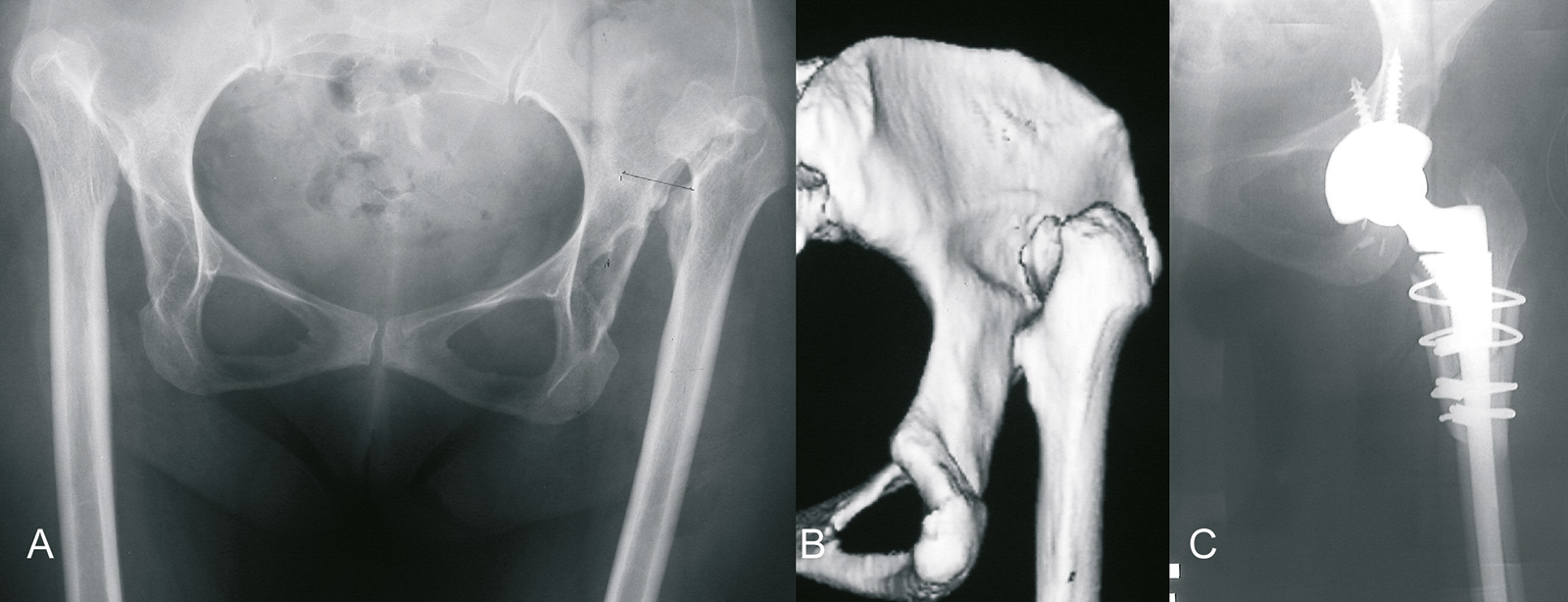
Verankerung:
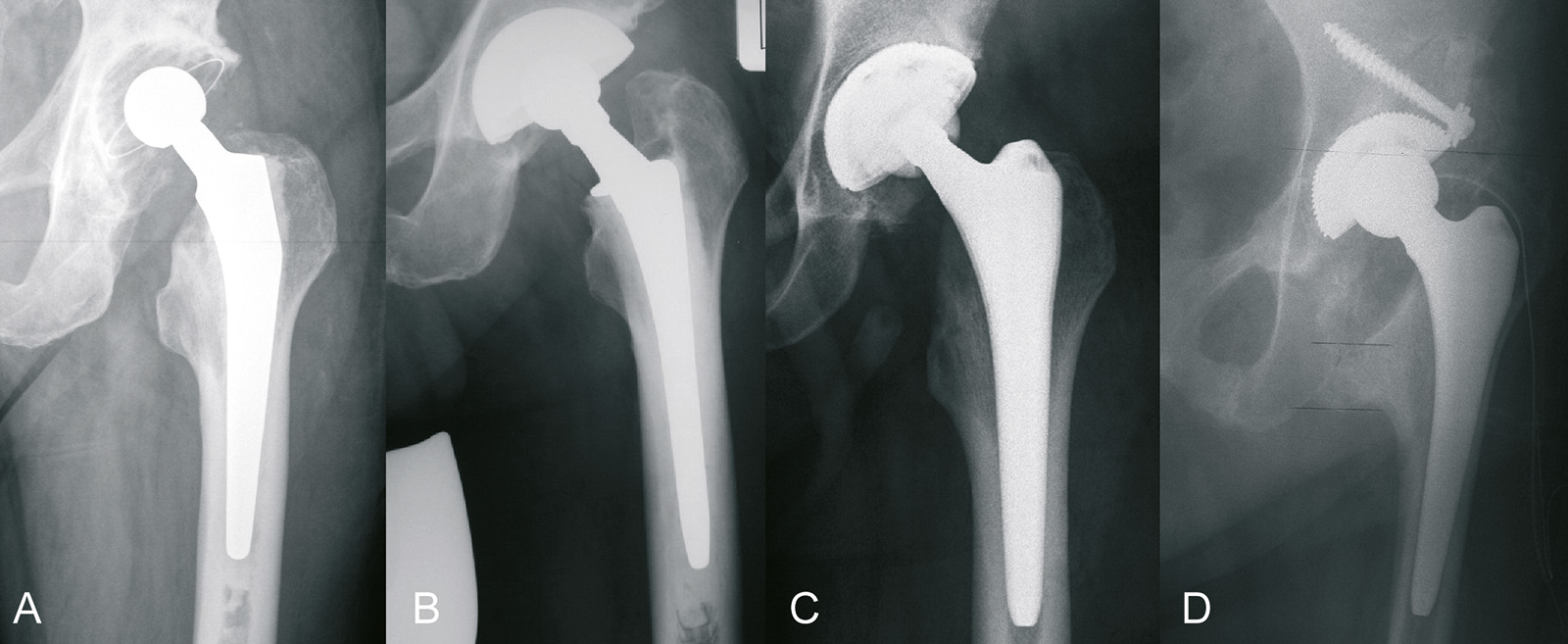
- zementierte Prothesen: Gold Standard in den 70-er bis Anfang der 90-er Jahre
- Hypothese: für starke zyklische Belastungen bei aktiven jungen Patienten ist eine zementfreie Verankerung mit der Möglichkeit zur biologischen Knochenadaptation vorteilhaft
- seit den späten 90-er Jahren:
- zementfreie modulare Pfannen werden heute bei fast allen Patienten implantiert
- es gibt einen eindeutigen Trend zu zementfreien Schäften: inzwischen haben Studien gute Ergebnisse auch bei älteren Patienten und Rheumatikern belegt
- zementierte Verankerung:
- Prothesenschaft: Verbesserungen der Zementiertechnik im Laufe der Jahre
- 1. Generation: der Zement wurde mit Fingern antegrad in den Markraum gefüllt und mit dem Daumen komprimiert („thumbing“)
- 2. Generation:
- Vorbereitung des Markraums mit einer Pulslavage-Spülung
- Ausstopfen des Kanals, um die Knochenoberfläche trocken zu legen
- Zementrestriktor: gestattet eine Kompression des Zements und verhindert ein Auffüllen des distalen Markraums
- Zement wird mit einer Zementpistole retrograd in den Kanal eingebracht
- 3. Generation:
- Zementmischung mit Vakuumpumpe, um Luftblasen im Zement zu minimieren, Verringerung der Porosität des Zements
- Komprimierung des Zements durch proximale Versiegelung in Kombination mit einem Zementrestriktor
- proximale und distale Kunststoffaufsätze, die ein zentrales Einbringen des Implantates ermöglichen (Centralizer)
- der optimale Zementmantel umgibt homogen das Implantat, hat eine Dicke von mindestens 2mm, enthält keine Luftblasen, hat keine Defekte und lässt ein Abgrenzen des Zementmantels vom kortikalen Knochen im diaphysären Bereich nicht zu (white out) (Klassifizierung nach Barrack A (white out) – D)
- zementfreie Verankerung:
- poröse Oberflächenstrukturen mit Porengrößen von 50-400μm (optimal: 50-150μm) gestatten ein Einwachsen des Knochens
- Oberflächenstrukturen werden erzeugt durch:
- „grid blasting“: Bestrahlung der Metalloberfläche
- Oberflächenbeschichtung mit kleinen Kugeln, die eine rauhe Oberflächenstruktur erzeugen (Problem: Kugeln können sich vom Implantat lösen)
- Hydroxyapatit Beschichtung: Kurzform „HA“, chemische Formel: Ca10(PO4)6(OH)2
- verbessert den Knocheneinwuchs (osteokonduktiv)
- Osteoblasten lagern sich der Oberfläche an und führen von beiden Seiten zu einem Einwachsen
- wird auf bestrahlte (grid blasting) oder unbestrahlte Oberflächen aufgetragen
- löst sich mit der Zeit auf, deswegen ist wahrscheinlich die Kombination mit einer rauhen Oberfläche günstiger
- ideale Schichtdicke: 50μm
- Prothesenschaft:
- proximale Anteile oder der gesamte Schaft
- nur proximaler Anteil der Prothese weist Oberflächenbeschichtung auf: gestattet proximale Fixierung und Lasteinleitung in die Femurmetaphyse
- gesamte Prothesenschaft ist beschichtet: fördert proximales Stress-shielding, da eine distale Krafteinleitung erfolgt; stress-shielding=Knochenresorption an nicht belasteten Arealen des Knochens: die Last wird durch das Implantat am proximalen Femur (Trochanter major und Trochanter minor) vorbei in den distalen Knochen eingeleitet, dies führt zu einer Osteopenie des proximalen Femuranteils
- Stress-Shielding wird verstärkt durch: hohe Steifigkeit und ein hohes Elastizitätsmodul des Implantats (Kobalt-Chrom > Titan), einen großen Implantatdurchmesser, eine ausgedehnte Oberflächenbeschichtung des Prothesenschaftes und durch das Schaftdesign
- Pfannenimplantate: gesamte Oberfläche weist Oberflächenstruktur auf
- Primärstabilität:
- Knochen wächst nur in Oberflächen ein, die fest mit ihm verbunden sind: Mikrobewegungen von mehr als 150μm verhindern ein Einwachsen des Knochens und fördern eine bindegewebige Interfacemembran
- Primärstabilität wird durch Press-fit Verankerung erreicht:
- Prothesenschaft: Knochenbett ca. 1-2mm kleiner als das Implantat (nur proximal oder auch distal, wenn eine distale Lasteinleitung gewünscht ist)
- Pfanne: hemisphärisch (über den gesamten Durchmesser) oder elliptisch (nur im Bereich des Pfannenrandes) ist das Implantat um 1-2 mm größer als das knöcherne Pfannenlager
- kortikaler Knochen gestattet eine festere Verankerung als spongiöser Knochen: Auswahl der richtigen Implantatgröße ist wichtig
Gleitpaarungen:
- Abrieb wird unterteilt in:
- Oberflächenabrieb (abrasive wear) aufgrund der Rauhigkeit der artikulierenden Oberflächen
- Haftungsabrieb (adhesive wear): durch Haftung artikulierender Oberflächen, werden kleine Bestandteile (Partikel) aus diesen Oberflächen herausgelöst
- Ermüdung (Fatigue): Risse im Kunstoff durch Belastungen der Oberfläche
- Abriebmodi: beschreibt Bedingungen, unter denen die Reibung erfolgt
- Modus 1: Abrieb erfolgt durch direkten Kontakt der Gelenkflächen
- Modus 2: eine Gelenkfläche reibt an einer Implantatoberfläche, die nicht als Gelenkpartner gedacht ist (meistens nach starkem Abrieb im Modus 1)
- Modus 3: ein Fremdkörper gelangt zwischen die Gelenkflächen und verursacht Abrieb
- Modus 4: zwei Oberflächen, die nicht Bestandteil des Gelenks sind, reiben aneinander (Rückfläche des Polyethyleneinsatzes gegen die Metallschale)
- Materialabrieb und sekundäre Osteolysen sind das Hauptproblem der modernen Endoprothetik
- Abrieb produziert kleine Partikel aus Polyethylen, Polymethylmethacrylat (PMMAKnochenzement), Kobalt-Chrom und Titan, die von Makrophagen phagozytiert werden
- die Makrophagen setzen Faktoren (Interleukine, Zytokine, Radikale, etc.) frei, die einen Knochenabbau einleiten
- langfristig führt dieser Prozess zum Verlust der Knochensubstanz (Osteolysen) und Lockerung des Implantates
- Partikel werden durch den hydrostatischen Druck im Gelenkraum verteilt und gelangen durch Schraubenlöcher in den acetabulären Knochen und in das Implantat-Zement- und das Zement-Knochen-Interface
- die Partikel, die durch Makrophagen phagozytiert werden, sind sehr klein: 0,2-7μm
- Polyethylen Partikel fördern den Knochenabbau am Stärksten
- Abrieb wird auch durch die Fähigkeit einer Oberfläche bestimmt, einen Flüssigkeitsfilm zwischen den Gelenkpartnern zu bilden, bessere Schmierung=weniger Reibung=weniger Verschleiss (Keramik bildet einen besseren Flüssigkeitsfilm als Metall)
- Polyethylen:
- Polymer aus dem Monomer Ethylen (C2H4)
- ultra-high-molecular-weight UHMW Polyethylen ist ein Polyethylen mit einem Molekulargewicht von mehr als 3 Millionen g/mol
- UHMW Polyethylen: Standard bis vor 10 Jahren
- 4 Verfahren zur Herstellung von UHMW Polyethlen
- ram bar extrusion und danach Bearbeitung in die gewünschte Form
- unter hohen Temperaturen und isostatischem Druck wird das PE Pulver in Stäbe (Bars) gepresst und dann weiter Verarbeitet
- Compression Molding (formen unter Druck) in PE-Bars und dann Weiterverarbeitung
- Direktes Compression Molding in die gewünschte Form
- Sterilisierung von Polyethylen: hat einen signifikanten Einfluß auf die Abriebeigenschaften
- die Sterilisation von Polyethylen mit Gammastrahlen unter Lufteinfluss führt zur Oxidation des Polyethylens und Abnahme der Vernetzung: das Ergebnis ist ein vermehrter Abrieb
- Sterilisation sollte im Vakuum erfolgen
- „nonenergetic“: durch chemische Verfahren (1) Gas-plasma Sterilisierung, (2) Ethylenoxid Sterilisierung
- „energetic“ durch Gammastrahlen: traditionelle Bestrahlung 2.5 bis 4.5 Mrad, neuere hochdosierte Bestrahlung mit 5 bis 15 Mrad
- seit 2000 hat sich hochvernetztes UHMWP als Standardmaterial durchgesetzt
- Vernetzung von benachbarten Polyethylenketten zu hoch vernetztem Polyethylen erfolgt durch Bestrahlung oder durch chemische Prozesse (historisch)
- Die durch Bestrahlung >5 Mrad in Abwesenheit von Sauerstoff erzielte Vernetzung von Polyethylen führt zur Verbesserung der Abriebeigenschaften
- Bestrahlung >5 Mrad produziert highly cross-linked Polyethylen
- Verringerung von „abrasive“ und „adhesive“ Abrieb
- Bestrahlung von UHMWP unter Sauerstoff führt zur Oxidation und damit zum Verlust von Abriebeigenschaften und sollte daher unbedingt vermieden werden
- PE besteht in 2 Phasen: amorph und krystalin, damit die Vernetzung erfolgreich ist muss die krystaline Phase 50-56% betragen
- Cross-linked UHMWP führt zu einer Verschlechterung der mechanischen Eigenschaften und verringert die Bruchfestigkeit (gemessen als „crack propagation“), dies kann zu Problemen führen, wenn Punktbelastungen auftreten (Impingement am Pfannenrand oder bei Knieprothesen mit geringer Konformität)
- damit durch die Bestrahlung freiwerdende Bindungen nicht oxidieren, wird das Material zumeist über den Schmelzpunkt von 135 Grad erwärmt, um sämtliche freien Radikale zu beseitigen; dies verändert die Ausrichtung der PE Ketten und kann Einfluß auf die mechanischen Eigenschaften haben, dieser Prozess heißt: Remelting
- manche Hersteller gehen darum nicht über den Schmelzpunkt sondern bleiben etwas darunter: <130 Grad, dieser Prozess heißt Annealing und hat einen geringeren Einfluß auf die mechanischen Eigenschaften (Stryker)
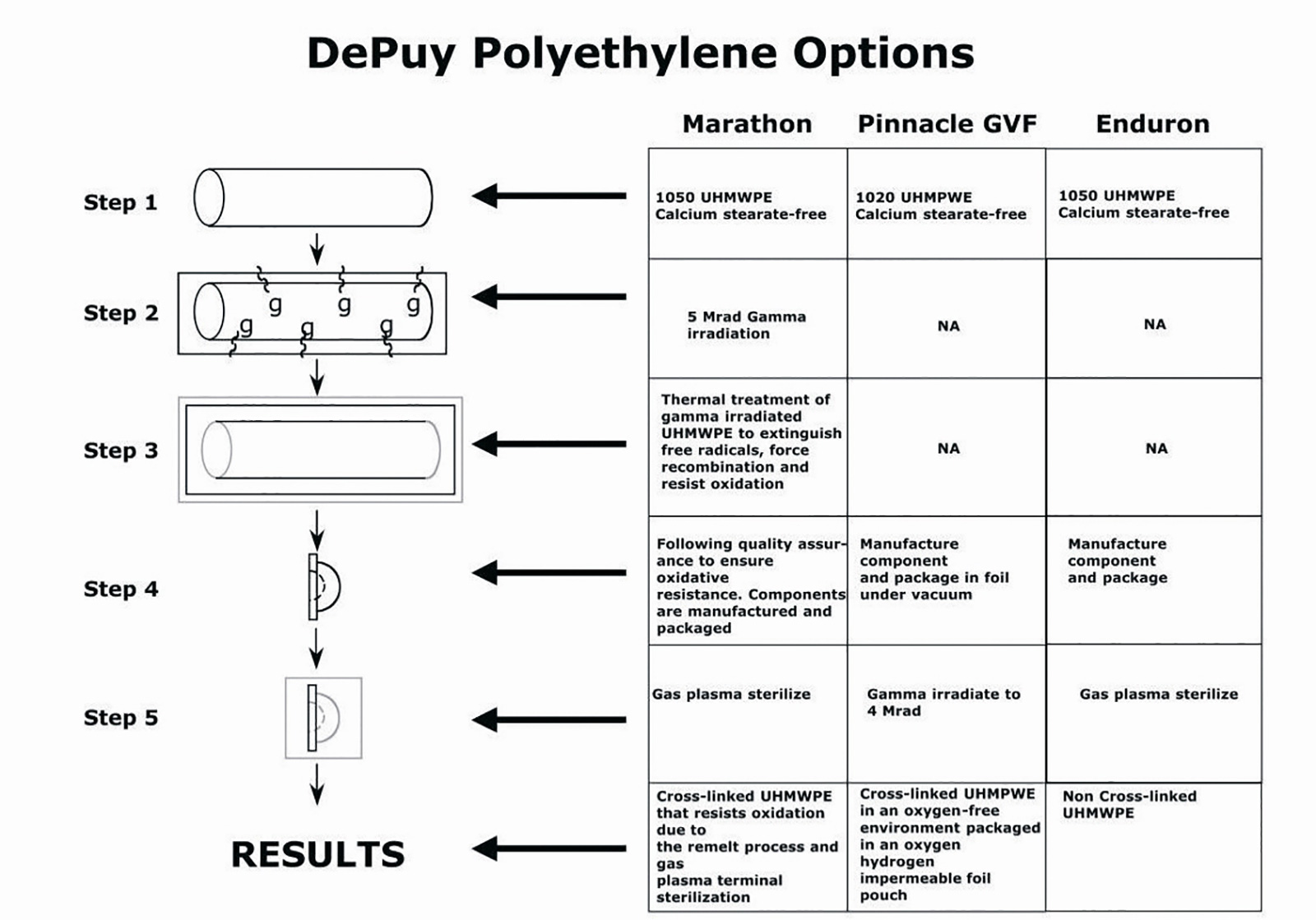
- Beispiele für hoch vernetzte Polyethylene sind: Marathon (DePuy), Longevity (Zimmer), Durasul (Centerpulse), Crossfire (Stryker), XLPE (Smith & Nephew); ArcomXLPE (Biomet)
- Eigenschaften hängen vom Ausgangsmaterial, Druck, Temperatur, Strahlendosis während der Herstellung und vom Herstellungsverfahren ab
- hoch vernetztes Polyethylen zeigt ein geringeres Abriebvolumen als ein vergleichbares UHMW-Polyethylen, jedoch eine erhöhte Brüchigkeit
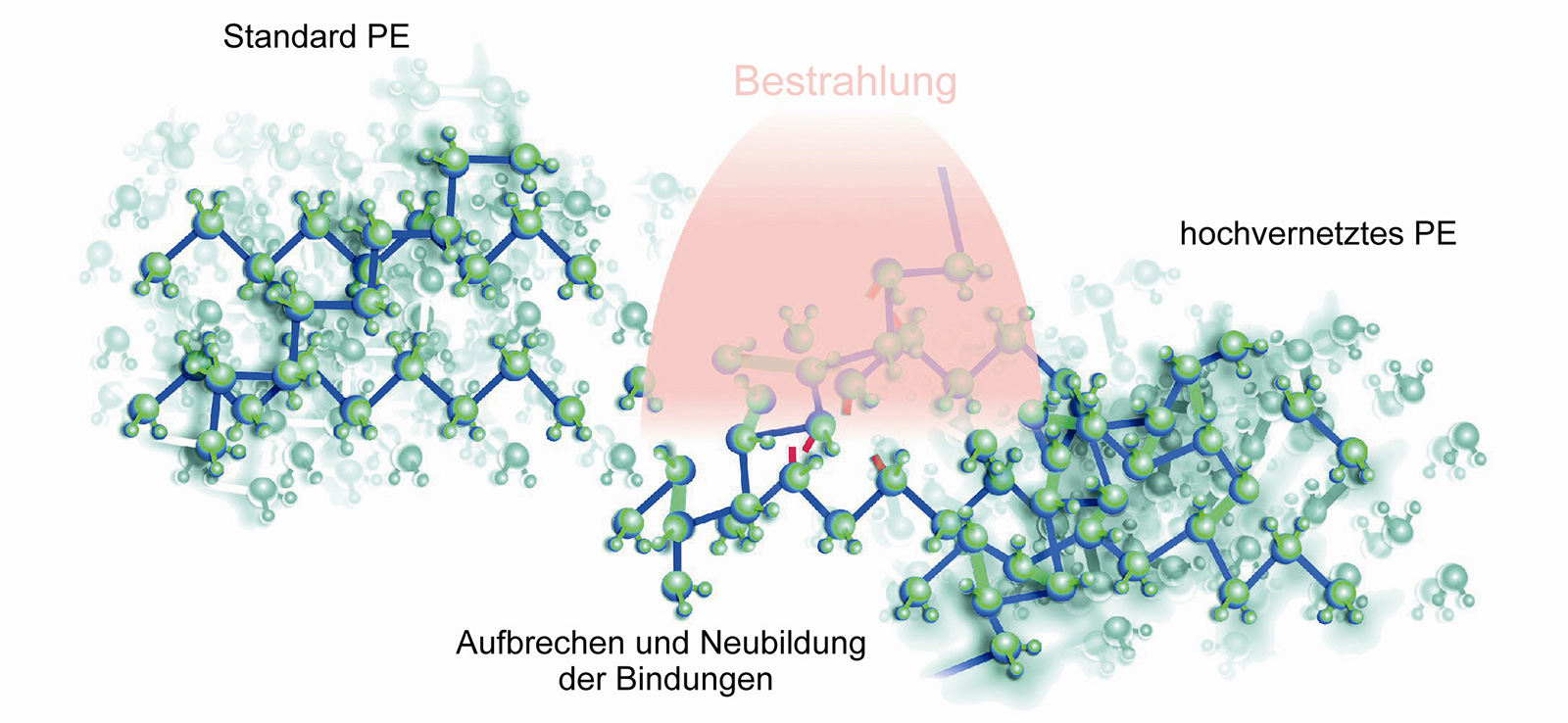
- Verpackung:
- Bestrahlung führt zur Bildung freier Radikale: werden UHWPE Produkte unter Sauerstoff bestrahlt oder verpackt führt das zur Oxidierung und Verlust der mechanischen Eigenschaften
- Bei langer Lagerung von hochvernetztem UHMWP difundiert Sauerstoff in das Material und führt zur Oxidierung
- Lagerungzeit von hochvernetzten UHMWP muss limitiert werden „shelf life time“, dies betrifft vor allem besonders kleine und große Größen, die seltener implantiert werden
- Vitamin E / Antioxidatien: einige Hersteller fügen heute Vitamin E Pulver oder andere Antioxidantien in das Ausgangs Polyethylenpulver, um die freien Radiakale zu binden, die bei der Bestrahlung entstehen
- es wird diskutiert, dass Vitamin E mit der Zeit aus dem Polyethylen difundiert und an Wirksamkeit verliertNeben Metall-Polyethylen und Keramik-Polyethylen gibt es auch „hard on hard“ Gleitpaarungen
- Keramik – Keramik
- Metall – Metall
- Metall – Keramik (neue Gleitpaarung mit relativ wenig Informationen)
- „hard on hard“ Gleitpaarungen führen zu weniger Abriebvolumen
- Keramik:
- zwei unterschiedliche Keramiksorten:
- Aluminiumoxid (Al2O3)
- Rate an Aluminiumoxidkeramikbrüchen liegt bei ca. 0.02% (1 auf 5 000 implantierte Keramik-Keramik Prothesen)
- Zirkoniumoxid (ZrO2): Ende der 90iger Jahre führten Veränderungen eines Herstellers (Saint-Gobain Ceramiques Avancees Desmarquest) in der Produktion von Zirkoniumoxid-Hüftköpfen zu einer Reihe an Kopfbrüchen, dieses Problem ist bei keinem anderen Hersteller aufgetreten, hat jedoch zu einer vermehrten Verwendung von Aluminiumoxidköpfen geführt
- Trend heute: Kombination des härteren Zirkoniumoxids mit Aluminiumoxid: Delta Keramik deutlich Bruch-fester, bis heute kein Deltakeramikbruch
- Keramik ist ein sehr hartes Material, es ist fast nicht möglich, die Oberfläche zu zerkratzen
- Knochenabbau aufgrund von Keramikpartikeln ist sehr selten beschrieben worden
- Keramik ist hydrophil und bildet einen exzellenten Flüssigkeitsfilm
- Probleme stellt heute vor allem die Verbindung des Keramikinlays mit der Metallschale der Pfanne dar: jede Verkantung beim Einbringen erhöht die Gefahr eines Keramikbruches
- extra lange Köpfe haben einen Sockel, der den Halsdurchmesser vergrößert und die Gefahr eines Impingements erhöht: es sollten keine Keramikköpfe mit einem solchen Sockel verwendet werden. Ausserdem ist dieser Sockel bruchgefährdet (die meisten Firmen bieten keine extra langen Keramikköpfe an)
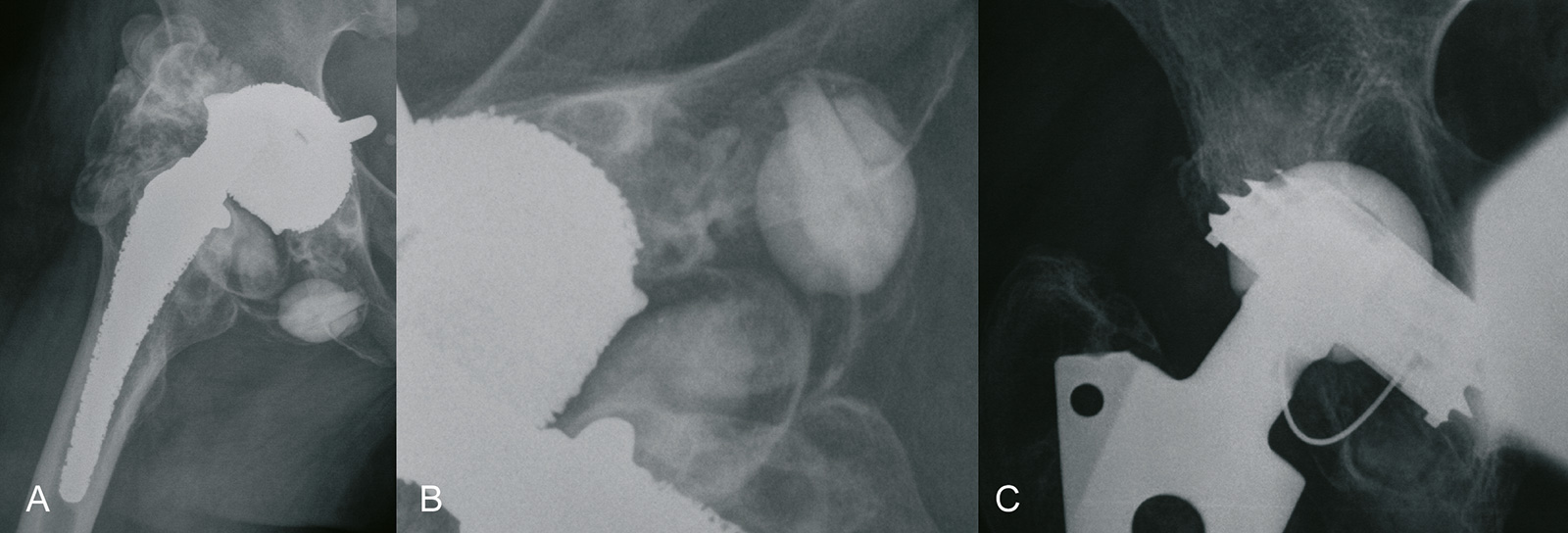
- Metall-Metall-Paarung:
- bis zu 200x geringeres Abriebvolumen als konventionelles Polyethylen
- deutlich mehr Abriebpartikel als konventionelles Polyethylen: Partikelgröße für MetallMetall Gleitpaarung (0.015-0.12μm) geringer als bei Polyethylen (0.2-7μm)
- ein größerer Kopfdurchmesser verursacht bei einer Metall-Metall Paarung weniger Abriebvolumen aber mehr Partikel
- je größer der Kopfdurchmesser, je glatter die Oberfläche und je besser das Design von Kopf und Pfanne ein Eintreten von Flüssigkeit zwischen die Gelenkpartner ermöglicht, um so besser der Flüssigkeitsfilm
- wahrscheinlich induzieren Metallpartikel in geringerem Umfang einen Knochenabbau als Polyethylenpartikel
- Metallpartikel sind kleiner als Polyethylenpartikel und können in größerer Anzahl in den Histiozyten gespeichert werden
- Metallionen-Konzentration in Serum, Urin und Erythrozyten ist bei Patienten erhöht, die eine Metall-Metall-Gleitpaarung haben: unklar ist, ob dies
- kanzerogen ist (nach dem skandinavischen Prothesenregister eher nein, jedoch ist eine Beurteilung erst nach vielen Jahrzehnten sicher möglich)
- zur Ausbildung einer Metall-Allergie führt
- bei entsprechenden Alternativen sollte bei folgenden Patienten auf eine Metall-MetallPaarung verzichtet werden:
- Frauen im gebärfähigen Alter
- heute sind Metall-Metall Prothesen nur im absoluten Einzelfall noch indiziert
- Patienten mit einer Niereninsuffizienz (verzögerte Ausscheidung der Metallionen)
- bekannte Metallallergie
- Metall – Metall Gleitpaarungen gehen mit deutlich erhöhtem Risiko für Pseudotumore und Gewebereaktionen auf die Metall-Gleitpaarung einher
- Pseudotumoren sind Gewebeproliferationen als Reaktion auf Metall Partikel
- Pseudotumor: Massive Osteolysen und Weichteildefekte als Ergebnis einer massiven synovialen Hypertrophie
- Implantate mit geringerer Klearance und geringerem Pfannenöffnungswinkel (ASR Metall-Metall Gleitpaarung, DePuy), schlechter Pfannenposition (zu steil oder antevertiert) haben höhere Versagerraten (Wechselraten bis 30% in den ersten 5 Jahren)
- Korrosion aufgrund von Metall Adaptern für verschiedene Kopfgrößen; erhöhen die Fehlerrate und sind wahrscheinlich die Ursache dafür, dass Hüftprothesen mit einer Metall-Metall Gleitpaarung höhere Fehlerraten aufweisen als Oberflächenersatzprothesen
- aufgrund der deutlich höheren Versagerrate wird heute ein jährliches Follow up empfohlen:
- asymptomatische Patienten mit normalen Metallion-Blutwerten <7ppb können jährlich verlaufskontrolliert werden (jährliches Röntgenbild)
- Cobalt- und Chromium Blutwerte von mehr als 7ppb sollten mit MRT /CT abgeklärt werden, um einen Pseudotumor auszuschliessen
- symptomatische Patienten müssen unabhängig von dem Metalionenwerten mit einem CT oder MRT untersucht werden
- bei symptomatischen Patienten mit zu steiler Pfanne >50-55 Grad (je nach Implantat) oder einem Implantat mit einer höheren Fehlerrate (ASR Hüfte) kann ein Prothesenwechsel nach Abwägung der Vor- und Nachteile diskutiert werden
- erhöhte Metallionenwerte allein stellen noch keine Indikation für einen Prothesenwechsel da (keine Korrelation zwischen Metalionen Blutwerten und Gewebezerstörung), jedoch sollte bei Werten von mehr als 30-50ppb mit dem Patienten die unklare medizinische Situation besprochen werden (es ist nicht klar ab welchen Werten Cobalt- und Chromionen toxisch sind)
Kopfgröße:
- beeinflusst das Verhältnis zwischen Kopf und Hals: je größer der Kopf, umso größer das Offset des Kopfes und umso größer der Bewegungsumfang bevor der Hals am Pfannenrand anschlägt (geringeres Luxationsrisiko); vorteilhaft: hohes Kopf-Hals-Verhältnis (Oberflächenersatzprothesen haben deswegen einen geringeren Bewegungsumfang als konventionelle Großkopfprothesen)
- je größer der Kopfdurchmesser, umso mehr Abriebvolumen entsteht
- je größer der Kopfdurchmesser, umso größer ist die Strecke, die der Kopf zurücklegen muss bevor er aus der Pfanne luxiert (geringeres Luxationsrisiko)
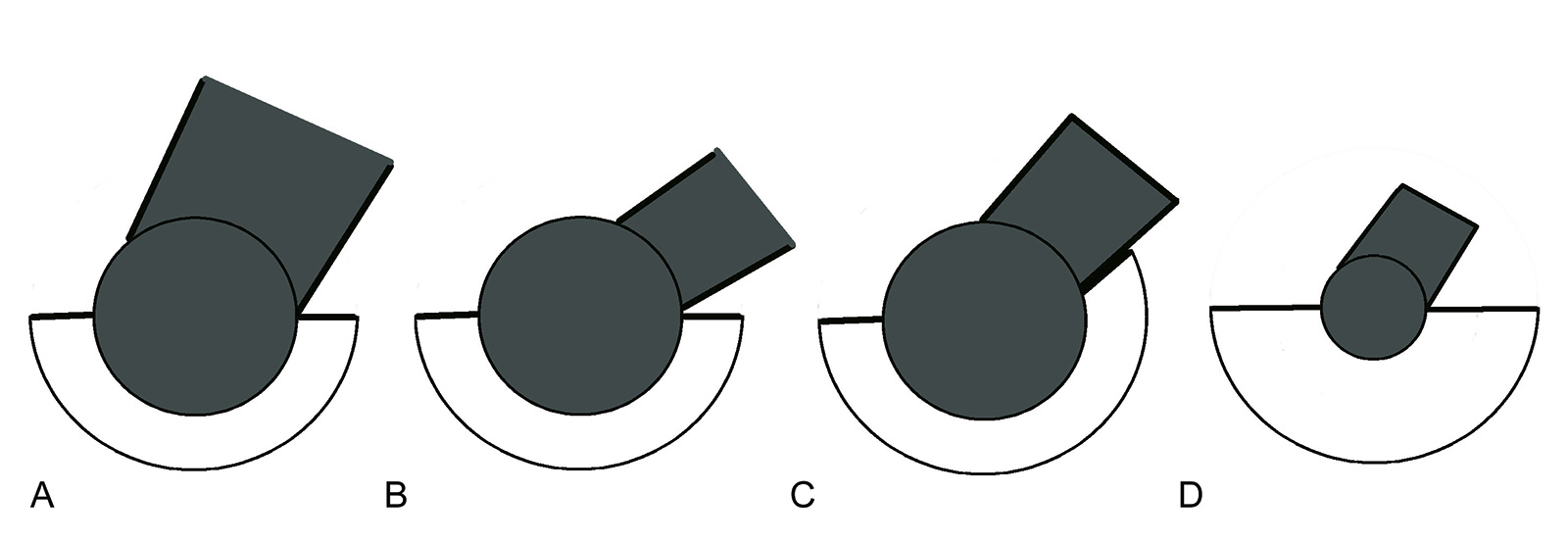
moderne Implantate:
- Ziel moderner Implantate ist die Lasteinleitung in das proximale Femur, um ein StressShielding zu vermeiden
- Femurdiaphyse wird für spätere Prothesenwechsel erhalten
- Beispiele:
- Oberflächenersatz als Hemi- oder Totalprothese
- Kurzschaftprothesen (Nano, Mini-Hip, ML-tapered stem, Trilock)

Operationstechnik:
- Navigation:
- Vermeidung von Fehlpositionierungen
- Navigation der Pfannenkomponente: für den weniger geübten Operateur sinnvoll, da die Pfannenposition einen großen Einfluss auf Abrieb, Bewegungsumfang, Impingement und das Luxationsrisiko hat
- Navigation des Prothesenschaftes: allenfalls zum Erreichen einer konstanten Beinlänge sinnvoll
- Technik: elektromagnetische-, Laser- oder Infrarot-Navigationssysteme
- Trend: Bildverstärker freie und CT freie Navigationssysteme
- Minimal invasive Operation:
- 2 Schnitte (Technik nach Berger): 5-6cm (je nach Pfannengröße) und 4cm
- Nachteile: Bildverstärker zur Lagekontrolle notwendig
- erhöhte Gefahr der Femurfraktur, da das Femur beim Raspeln nicht eingesehen werden kann (bis zu 7% in Studien)
- längere Operationszeit
- Summe aus der Schnittlänge beider Schnitte größer als beim hinteren oder anterolateralen Zugang
- Vorteil: Dr. Berger (Chicago) beschrieb erste ambulante Hüftoperation, es ist wahrscheinlich, dass die anterioren Zugänge eine schnellere Frührehabilitation ermöglichen
- Nachteile: Bildverstärker zur Lagekontrolle notwendig
- hinterer Zugang:
- Schnittlänge: 7-10cm
- Nachteil: Luxationsrisiko erhöht, wenn die Außenrotatoren und Kapsel nicht refixiert werden (Luxationsrisiko 4 % ohne Refixierung versus 1% mit Refixierung)
- Vorteil: exzellenter Zugang für spätere Wechseloperationen, bessere Planung der Beinlänge aufgrund besserer Darstellung des Trochanter minor, Abduktoren bleiben unberührt
- anterolateraler Zugang nach Harding:
- Schnittlänge: 10cm
- Gluteus medius wird abgelöst, Gefahr postoperativen Hinkens erhöht
- anterolateraler Zugang (Technik nach Röttinger, OCM Zugang):
- Schnittlänge: 6-10cm
- schont den Gluteus medius (Zugang zwischen Tensor fascia lata und Gluteus medius)
- anteriorer Zugang in der Technik nach Judet, Mata, etc.:
- Schnittlänge: 7-10cm
- Zugang zwischen Tensor fascia lata und Sartorius
- es werden keine Muskeln abgelöst
- geringes Luxationsrisiko (1%)
- Vorteile einer minimal invasiven Implantation:
- Verringerung des Blutverlustes
- Verkürzung der postoperativen Rehabilitation in den ersten 6 Wochen, nach 6 Monaten kein Unterschied
- Verkürzung des stationären Aufenthaltes
- Nachteile:
- Gefahr der Fehlpositionierung: Kombination mit Navigation der Pfannenimplantation ist sinnvoll
- minimal invasive Zugänge sind technisch anspruchsvoll, in der Lernphase erhöhte Komplikationsrate
- 6-12 Wochen nach der Operation haben Patienten, die über einen minimal invasiven Zugang operiert wurden, und Patienten, die über einen Standardzugang operiert wurden, das gleiche Funktionsergebnis
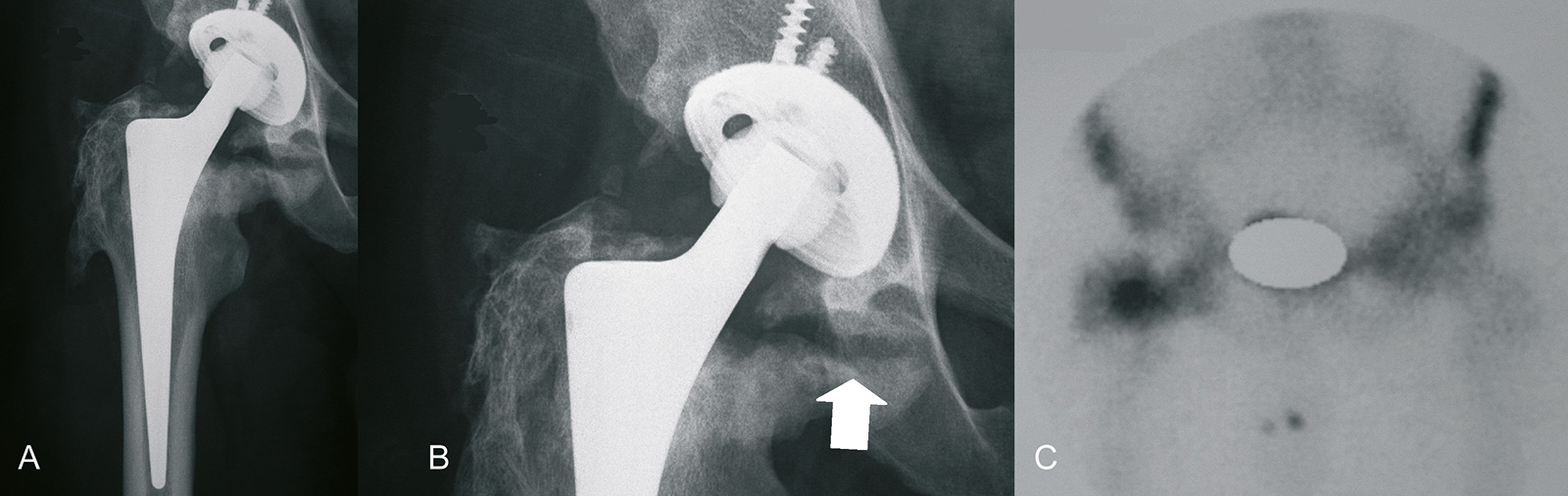
Ergebnisse:
- die primäre Hüftprothesenimplantation hat exzellente Ergebnisse: im Durchschnitt liegt die Wechselrate nach 10 Jahren für zementfreie und zementierte Schäfte und für zementfreie Pfannen bei unter 5%
- Funktion:
- Treppensteigen: vor Entlassung aus dem Krankenhaus
- 2 Gehstützen, 1 Gehstütze, Gehstock, freies Gehen: das Gehen ohne Hilfsmittel sollte in den ersten 6 Wochen möglich sein
- Duschen: sobald die Klammern entfernt sind, meistens nach 12 Tagen (kein Bürsten oder Einseifen der Wunde)
- Autofahren: nach 8 Wochen sind Reaktionszeiten und Kraft vergleichbar mit Normalbevölkerung
- Sport mit starker Belastung sollte möglichst vermieden werden, höhere Lockerungsraten nach 10 Jahren: Joggen, Tennis, Rucksackwandern, Squash, Handball, Reiten, schwere körperliche Arbeit
- Sport mit geringer Belastung wird empfohlen: Schwimmen, Radfahren, Wandern, Golf, Ski (erfahrener Skifahrer), Kegeln, Doppel (Tennis)
- Sex: ca. 50 % sind nach 1-2 Monaten wieder sexuell aktiv
- das endgültige Funktionsergebnis wird nach zirka 3-6 Monaten erreicht
- Prothesenwechsel:
- mit der Anzahl der Prothesenwechsel nimmt das zu erwartende Funktionsergebnis ab
- etwa 15 % aller Hüftprothesenoperationen sind Wechseloperationen
Komplikationen:
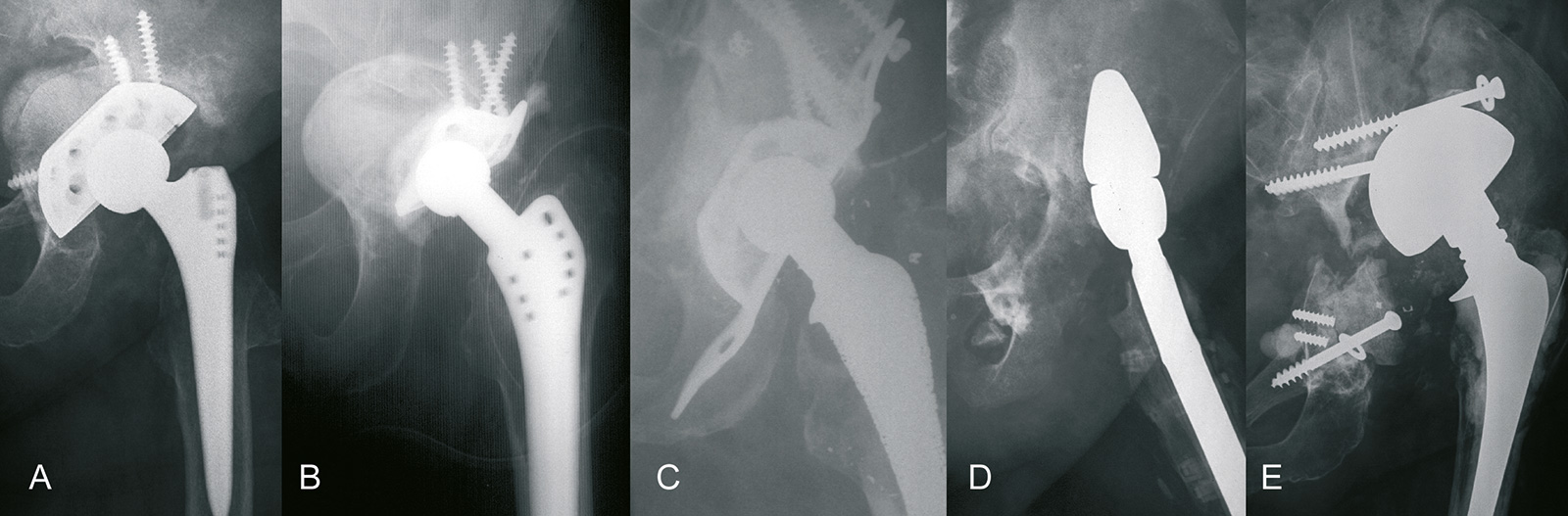
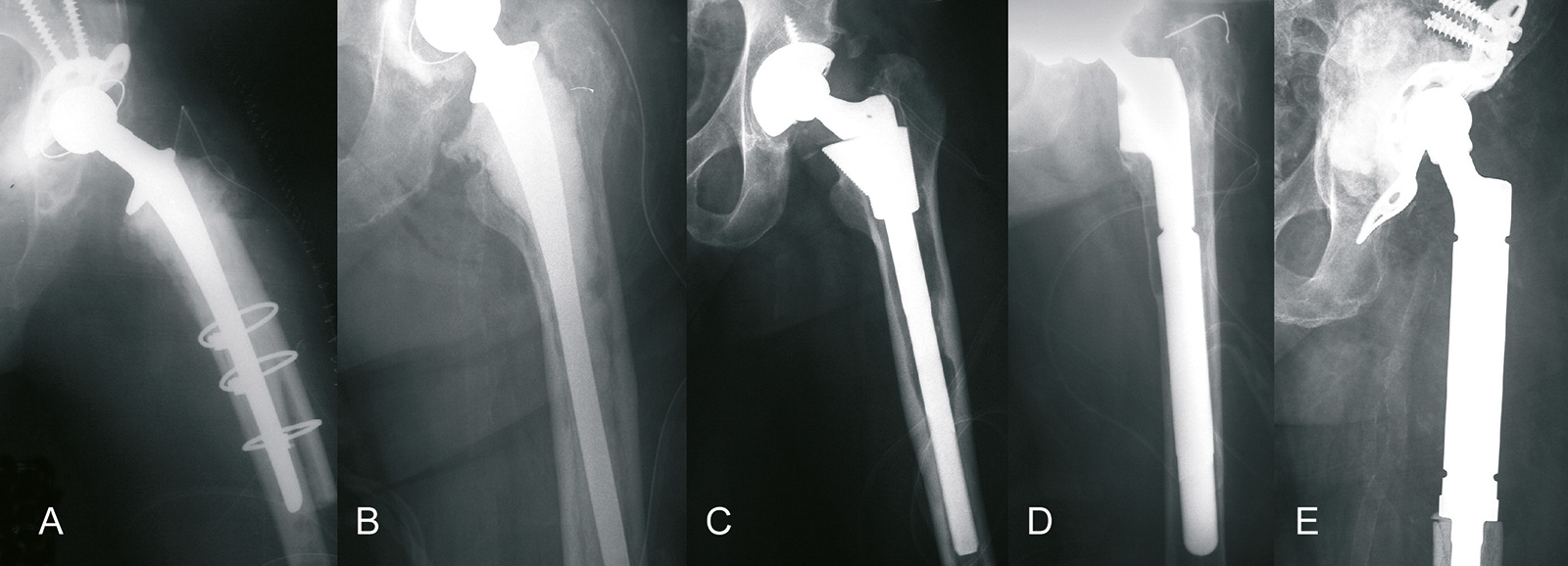
- Schaftschmerz: nach Implantation zementfreier Prothesen (5% der Patienten), v.a. bei distal nach dem fit-and- fill Prinzip verankerten Prothesen (Markraum wird mit Prothese ausgefüllt), oft Besserung innerhalb von 2 Jahren
- tiefe Infektion:
- intraoperative Prophylaxe während der Prothesenimplantation: Cefazolin 1-2 g (Dauer der Gabe: 24 Stunden)
- Risikofaktoren: rheumatoide Arthritis (x3), Diabetes mellitus (x2), Sichelzellanämie, Dialyse, Hämophilie, HIV, Übergewicht (?), Prothesenwechsel > Primärimplantation
- Einteilung nach Coventry:
- Phase 1: < 6 Monate nach Operation (akute Infektion)
- Phase 2: 6-24 Monate nach Operation (chronische Infektion durch Keime mit geringer Virulenz)
- Phase 3: > 24 Monate (späte hämatogene Infektion)
- Diagnose:
- Blutbild Leukozyten: Sensitivität 20 %, Spezi tät 96 % (keine Bedeutung)
- Blutsenkung: Sensitivität 82 %, Spezifität 85 % (keine Bedeutung)
- CRP: Sensitivität 96 %, Spezifität 92 % (beste Marker)
- Interleukin 6: in Kombination mit der CRP zur Erhöhung der Sensitivität
- Knochenszintigrafie: sensitiv aber nicht spezifisch (keine Bedeutung)
- Punktion: >15 000 Leukozyten/ml, positive Kultur (Punktion, wenn der Patient 2 Wochen ohne Antibiotika) (Punktion indiziert bei allen Patienten mit erhöhter CRP oder Interleukin 6)
- intraoperative Kultur: wenn mehr als 3 Proben entnommen werden
- 0 von 3 Kulturen positiv: Infektrisiko < 3 %
- 1 von 3 Kulturen positiv: Infektionsrisiko 13.3 %
- 2 von 3 Kulturen positiv: Infektionsrisiko 30 %
- 3 von 3 Kulturen positiv: Infektionsrisiko 95 %
- entscheidend ist es mehrere Gewebs- und Flüssigkeitsproben einzuschicken
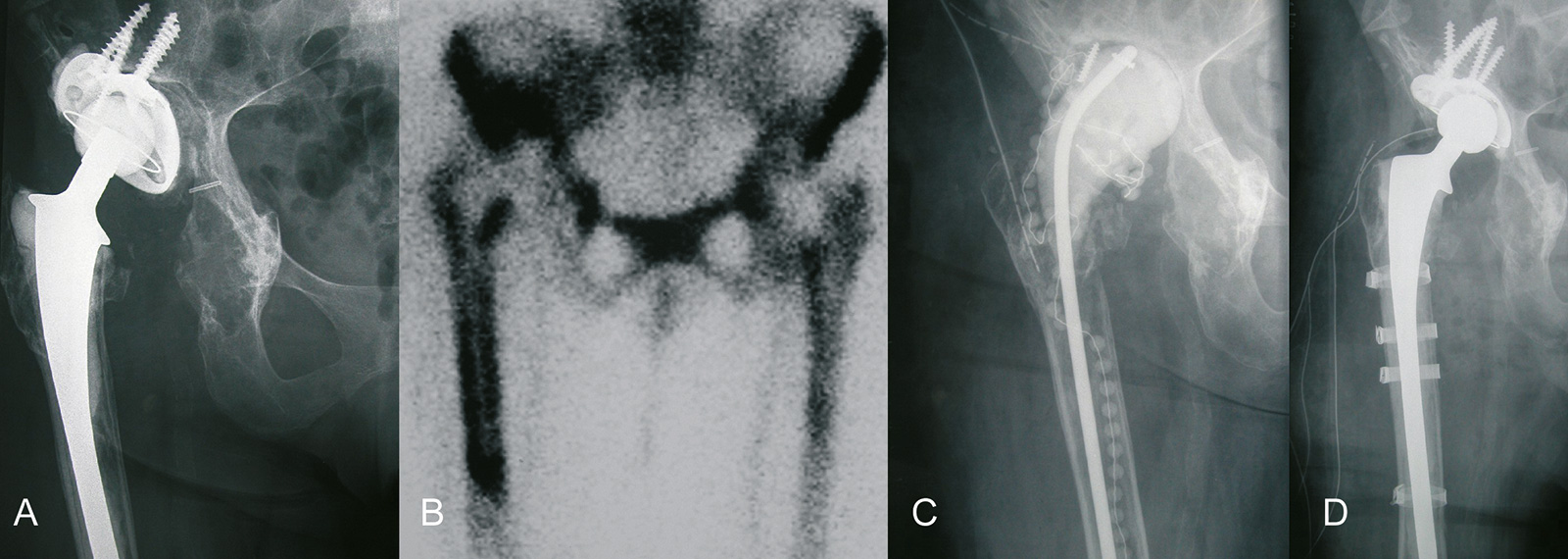
- Therapie
- 2-zeitiger Wechsel:
- Prothesenausbau und Antibiotika-Zementplatzhalter
- dann 2-6 Wochen intravenöse Antibiose nach Resistogramm
- Reimplantation einer neuen Hüftprothese nach frühestens
2 Wochen (nach Normalisierung der CRP und negativer Punktion), in der Literatur wird ein Intervall von 6 Wochen empfohlen, Punktion vor Reimplantation erfolgt 2 Wochen nach letzter Antibiotikagabe - Reinfektion < 10 % der Fälle
- Methode der Wahl
- 1-zeitiger Wechsel:
- Indikation: sensibler Keim, kurze Anamnesedauer, gute Weichteildeckung, keine
Fistel - Ausbau und Reimplantation während einer Operation
- Reinfektion in ca. 20 % der Fälle
- Indikation: sensibler Keim, kurze Anamnesedauer, gute Weichteildeckung, keine
- Débridement ohne Prothesenwechsel:
- Reinfektion in ca. 40 % der Fälle
- Girdlestone Resektionsarthroplastik:
- Prothese wird ohne Ersatz entfernt
- erneute Infektion in ca. 15% der Fälle
- schlechte Funktion: Beinverkürzung, Hinken, Schmerzen
- 2-zeitiger Wechsel:
- tiefe Venenthrombose:
- klinische Zeichen sind weder sensitiv noch spezifisch für eine Thrombose
- Doppler-Ultraschall ist das Diagnoseverfahren der Wahl
- MRV (Magnet-Resonanz-Venografie): zum Nachweis von Beckenvenenthrombosen
- Risikofaktoren: Alter, Tumorleiden, Herzinsuffizienz, Übergewicht, Immobilisierung,
Blutgruppe A, orale Antikonzeptiva, Rauchen - Risiko wird gesenkt durch: Regionalanästhesie, Operationszeit <70 Minuten, prä-
operative Eigenblutspende, Thromboseprophylaxe (niedrigmolekulares Heparin,
Marcumar, pneumatische Kompressionspumpen, Kompressionsstrümpfe, intraoperative
Gabe von Heparin (10 IU/ kg KG)) - Schaftpräparation: Positionierung des Beins in Flexion, Adduktion und Innenrotation
führt zu einem Verschluss der venösen Strombahn (während der Operation sollte das
Bein nur so kurz wie möglich in dieser Position verbleiben)
- Lungenembolie:
- Tachypnoe, Dyspnoe, Tachykardie, Verringerung des pO2 (Blutgase)
- Spiral CT: heute Methode der Wahl (früher Ventilations-Perfusions-Szintigrafie)
- tödliche Lungenembolien: 1-2/1000 Hüftprothesenimplantationen
- Blutverlust: Fremdbluttransfusionen können vermieden werden durch
- Eigenblutspende (1 Konserve)
- perioperative Cell-Saver: anstelle der Eigenblutspende und bei aseptischen Wechseloperationen indiziert
- hypotensive Anästhesie
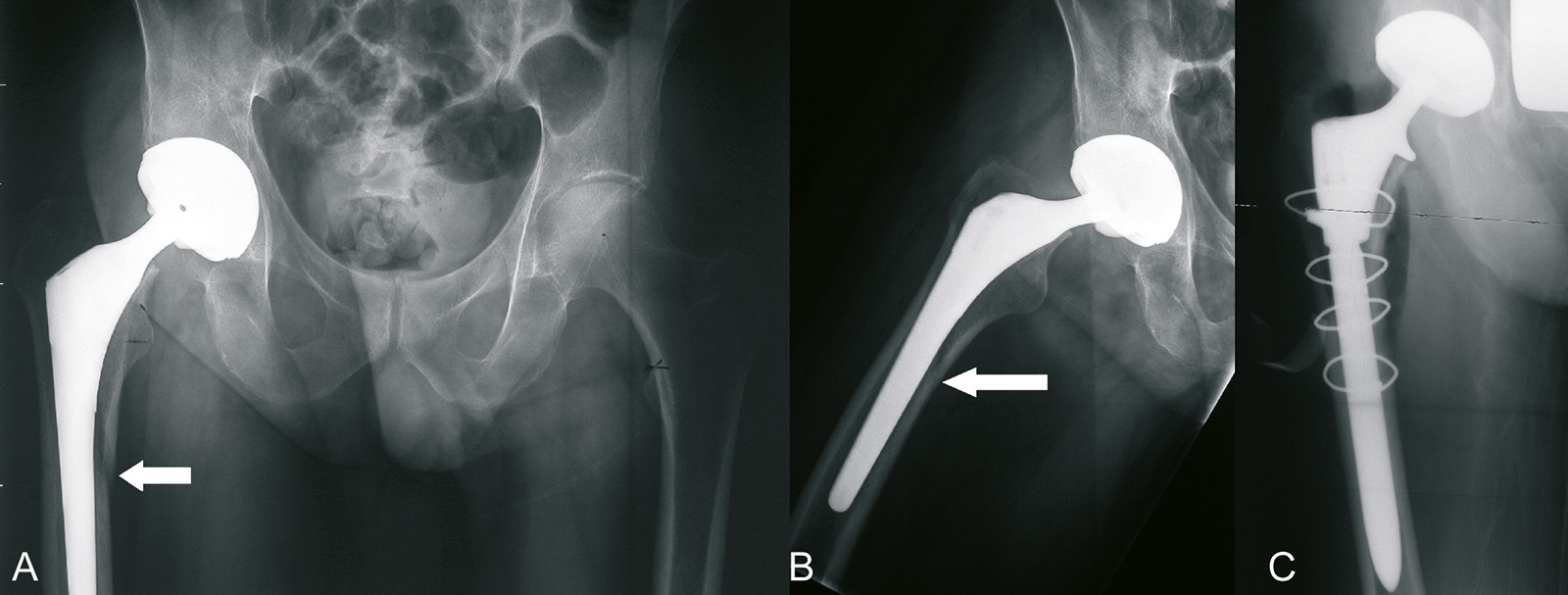
- periprothetische Fraktur:
- zementfreie Prothesen: Frakturen treten in den ersten 6 Monaten und intraoperativ auf
- zementierte Prothesen: Frakturen treten meistens erst nach 5 Jahren auf
- Prothesenwechsel, wenn die Verankerung der Prothese beeinträchtigt ist
- Vancouver Klassifikation:
- Typ A: Fraktur des Trochanter majors oder minors
- Typ B: Fraktur entlang des Prothesenschaftes (B1: Prothese gut fixiert, B2: Prothese
locker, B3: unklar) - Typ C: Fraktur distal des Prothesenschaftes
- Nervenverletzung: 0.5-2% aller Fälle
- Risiko ist erhöht bei Patienten mit einer primären Prothesenimplantation aufgrund einer
Hüftdysplasie und -luxation (5%) und bei Wechseloperationen (3.6%) - beim anterolateralen Zugang zwischen Tensor fascia lata und Gluteus medius ist der
N. gluteus superior gefährdet (Insuffizienz der Abduktoren) - beim hinteren Zugang: N. ischiadicus; N.-peroneus-Anteil des N. ischiadicus ist am
häufigsten betroffen; Prophylaxe: keine Beinverlängerung um >4cm - Erholung meistens in den ersten 7 Monaten, N. gluteus superior schlechte Prognose,
führt zu positivem Trendelenburg
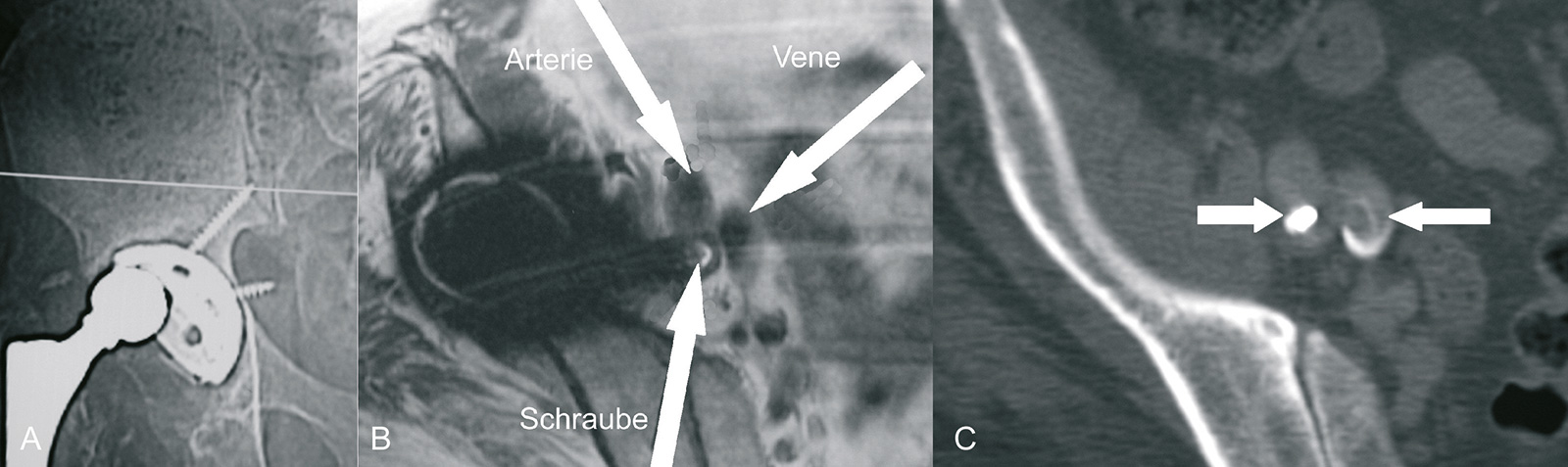
- Gefäßverletzung: selten
- heterotope Ossifikationen:
- Risikofaktoren:
- ausgeprägte Osteophytenbildung vor Prothesenimplantation
- M. Bechterew
- posttraumatische Arthrose
- Z.n. Hüftarthrodese
- Prophylaxe: NSAR (Indomethacin 3x50mg für 14 Tage) oder einmalige Bestrahlung
- Brooker Klassifikation:
- Grad 1: einzelne Inseln heterotopen Knochens
- Grad 2: Knochenanbauten an Acetabulum und Femur mit einem knochenfreien
Übergang von wenigstens 1cm - Grad 3: weniger als 1cm knochenfrei zwischen den heterotopen Knochenanbauten
- Grad 4: komplette Knochenbrücke zwischen Femur und Acetabulum
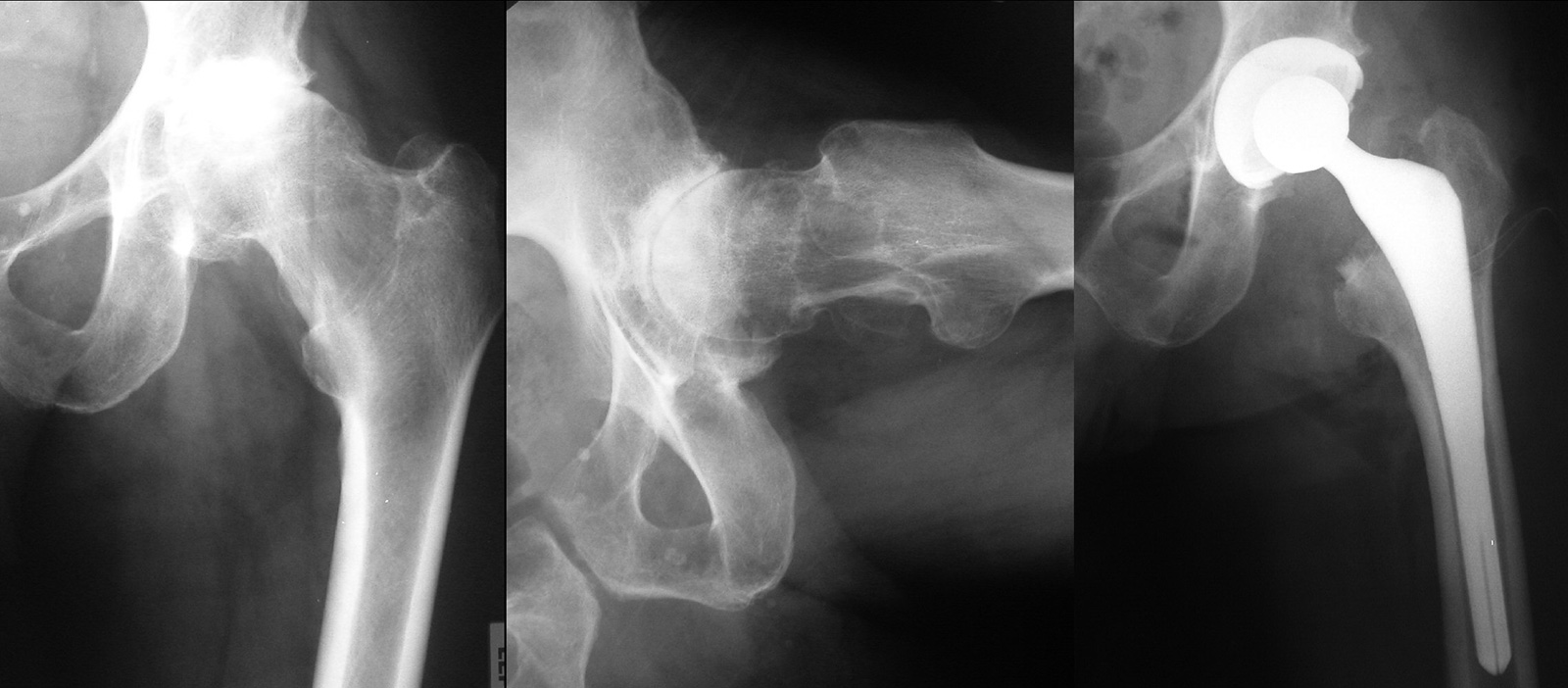
- Hüftgelenksluxation:
- Inzidenz: ca. 1-4%
- Risikofaktoren: anterolateraler Zugang (1%), hinterer Zugang (1-4%), ältere Frauen,
Wechseloperation (bis zu 10%), cerebrale Begleiterkrankungen (M. Parkinson, etc.) - Klinik: Schmerz, Beinverkürzung, Innenrotation (hintere Luxation) oder Außenrotation
(vordere Luxation) - Ursache: Fehlpositionierung der Pfanne und/oder des Schaftes, Insuffizienz
der Hüftabduktoren (Prothesenwechsel, Trochanterfraktur), Impingement des
Prothesenhalses oder des proximalen Femurs (Trochanter) an der Pfanne oder dem
Acetabulum (Osteophyten), fehlende Compliance des Patienten - Prophylaxe: korrekte Ausrichtung der Prothesenkomponenten (Navigation),
Wiederherstellung der Beinlänge (adäquate Weichteilspannung), Wiederherstellung
des Offsets zwischen Kopf und Trochanter, Verringerung des Impingements
zwischen Prothesenhals und Pfanne durch Verwendung schmalerer Hälse mit einem
trapezförmigen Querschnitt und einem großen Kopf-Hals-Verhältnis - Therapie:
- Korrektur einer Komponentenfehlpositionierung ist in 70% der Fälle ausreichend, bei
einer Fehlstellung der Pfanne sollte diese zuerst korrigiert werden - aktuelle Literatur zeigt für gekoppelte Pfannen (constrained Liner) die besten
Langzeitergebnisse - Alternative: Verwendung großer Köpfe (Durchmesser, 32, 36 oder 44mm)
- Korrektur einer Komponentenfehlpositionierung ist in 70% der Fälle ausreichend, bei
