Ewingsarkom
- maligner Tumor, wahrscheinlich neuroektodermalen Ursprungs, charakterisiert durch dicht gepackte kleine Zellen mit runden Kernen
- Alter: 5. – 30. Lebensjahr
- Jungen > Mädchen
- Lokalisation: metaphysennahe Diaphyse langer Röhrenknochen (Femur, Tibia, Fibula, Wirbelsäule)
- Einteilung:
- Ewing-Sarkom
- peripherer (primitiver) neuroektodermaler Tumor (PNET): Translokation 11/22 und MIC 2 Gen wie bei Ewing-Sarkom; makroskopisch nicht zu unterscheiden; mikroskopisch: zusätzlich neurogene Differenzierung: Nachweis von mindestens 2 neurogenen Markern (S100, NSE, Synaptophysin etc.); schlechtere Prognose als Ewing
- Askin-Tumor der Brustwand
- peripheres Neuroepitheliom
- Verlauf:
- wahrscheinlich neuroektodermalen Ursprungs (positiv für Neuronen spezifische Enolase NSE), sowohl differenziertere Formen (PNET) als auch weniger differenzierte Formen (klassisches Ewing Sarkom)
- anfänglich Ausbreitung im Markraum ohne Einbruch in den Knochen
- infiltriert die Haverschen Kanäle und hebt das Periost ab
- reaktive mehrschichtige Periostverkalkungen (Zwiebelschalenmuster)
- später Infiltration der Periostreaktion und Ausbildung einer ausgedehnten Weichteilkomponente
- frühe Metastasierung vor allem hämatogen in die Lunge, zum Diagnosezeitpunkt haben ¼ der Patienten Metastasen
- unbehandelt entwickeln 90% innerhalb eines Jahres Lungenmetastasen und versterben später an den Folgen der Lungenmetastasierung
Ätiologie:
unklar, 95% haben Mutation des Chromosom 22 (11/22 Translokation)
Klinik / Diagnose:
- Fieber, Abgeschlagenheit, Gewichtsverlust
- Schmerz, Druckschmerzhaftigkeit
- teilweise rasante Größenzunahme
- Labor: BSG und LDH oft erhöht
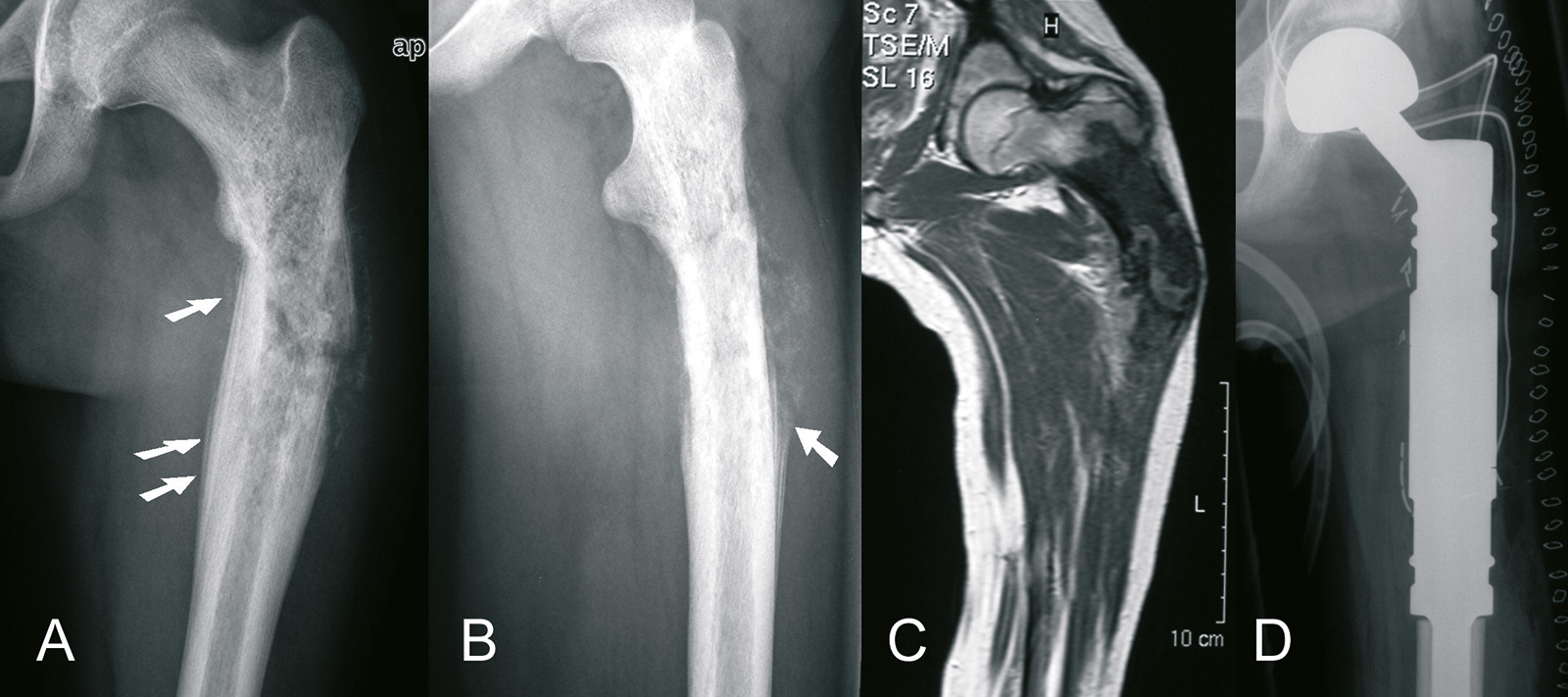
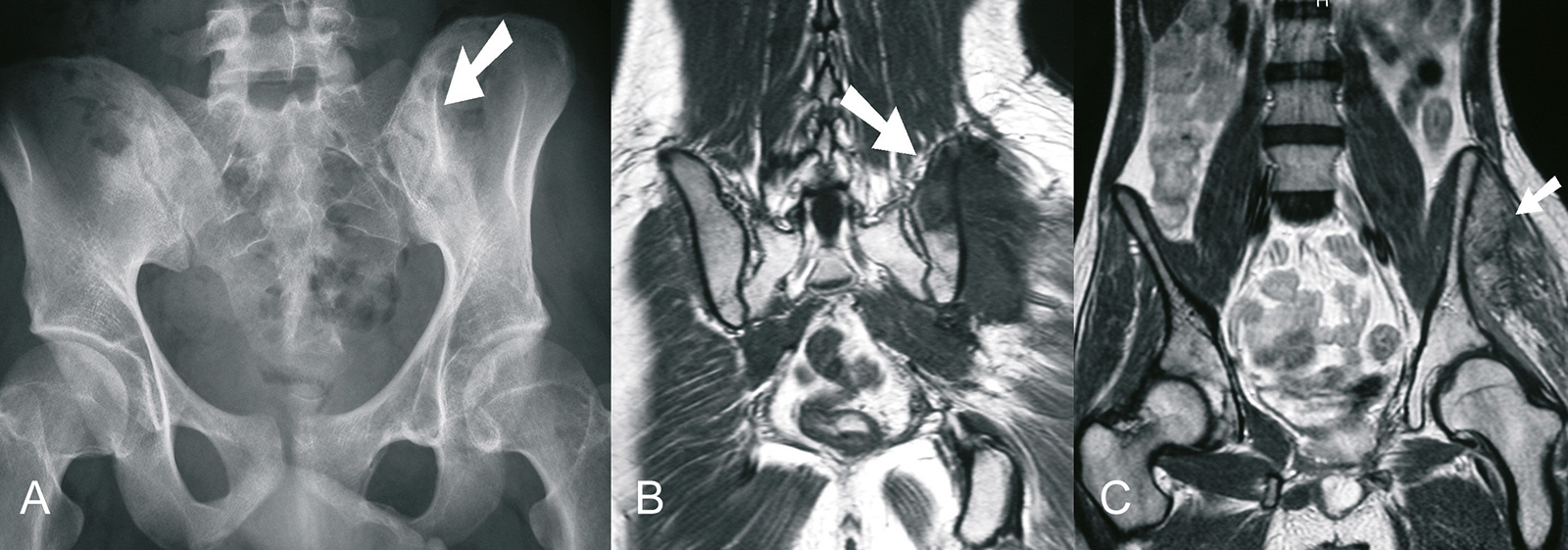
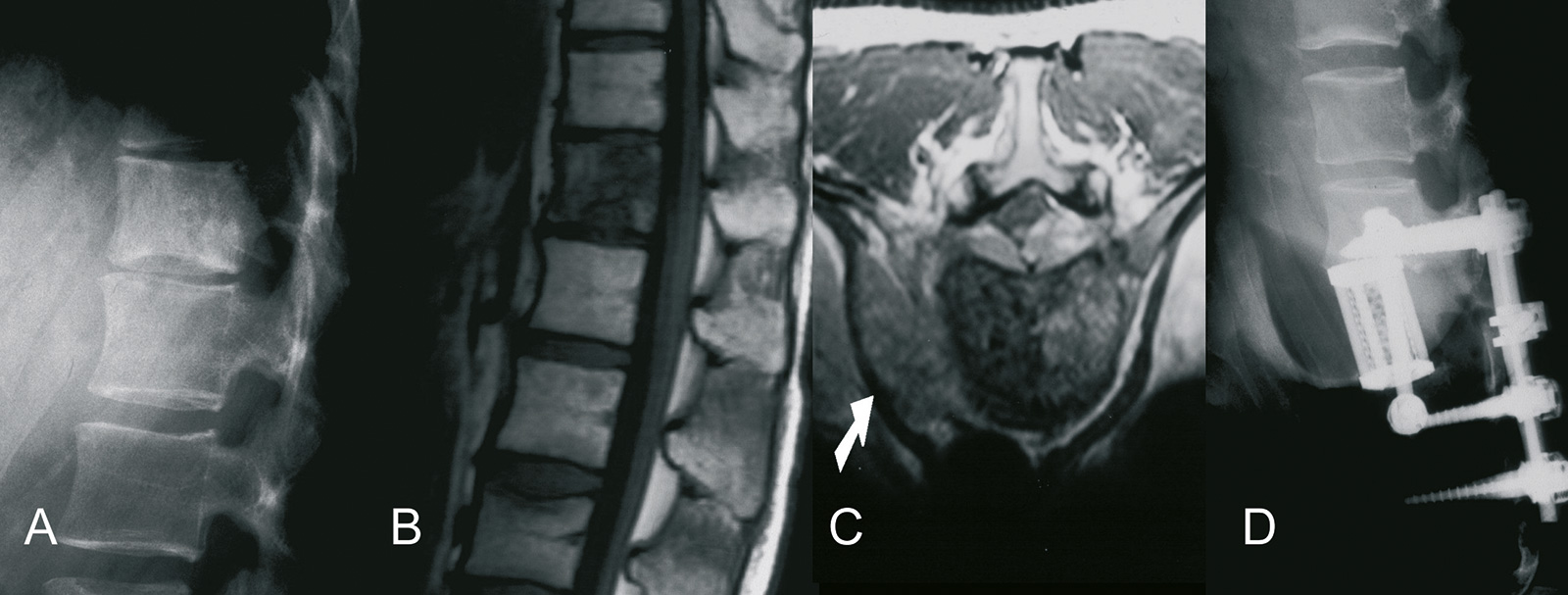
- Röntgen:
- initial: unscharf begrenzte Osteolyse im Markraum
- mit Fortschreiten der Erkrankung: Zwiebelschalenmuster (verkalkte Periostlamellen)
- und deutliche Weichteilkomponente mit Codman-Dreiecken
- Knochenszintigrafie:
- Mehranreicherung, die deutlich über die radiologisch sichtbaren Grenzen der Läsion hinausgeht
- Computertomografie:
- Tumorausdehnung, Weichteilkomponente, jedoch ist eine genaue Abgrenzung für die Planung der Tumorresektion im CT nicht möglich (MRT Methode der Wahl)
- Kontrastmittelenhancement
- lokale Lymphknotenmetastasen
- CT heute nur selten indiziert
- MRT: (Methode der Wahl)
- T 1: intermediäre Intensität
- T 2: hyperintense Läsion
- Histologie:
- makroskopisch: grau-weißes Tumorgewebe, gefäßreich
- mikroskopisch: kleine, runde Zellen mit wenig basophilem Zytoplasma (klein-blaurundzelliger Tumor); Glykogen im Zytoplasma zu Pseudorosetten zusammengelagert; Nekrosen & Einblutungen; wenige Mitosen; Vimentin positiv, expremiert MIC 2 Gen
- Staging-Untersuchungen: CT-Thorax, CT-Abdomen, 3-Phasen-Knochenszintigra-phie, Knochenmarkstanze
- Differentialdiagnose:
- Osteomyelitis: kurze Anamnese (<2 Wochen), metaphysäre Lage, Periostlamellen sind nicht unterbrochen, Focus (Tonsillitis, Lungenentzündung, Zahnabszess), CRP erhöht
- eosinophiles Granulom: geringere Weichteilkomponente, geringere Symptomatik, Szintigrafie: weitere Läsionen?
- kleinzelliges Osteosarkom: Verkalkung der paraossalen Tumormatrix als Hinweis auf Osteoidbildung
- Non-Hodgkin Lymphom: Anamnese & Staging
Therapie:
- Inzisionsbiopsie
- Therapie erfolgt entsprechend den Leitlinien der EURO-EWING 1999 (European Ewing
Tumour Working Initiative of National Groups Ewing Tumour Studies 1999):
- Studienzentrale:
Westfälische-Wilhelms-Universität Münster
Klinik für Kinderheilkunde
Pädiatrische Hämatologie/Onkologie
Albert-Schweitzer-Str. 33
48149 Münster
Tel.: 0251-835-6489
e-mail: ewing@uni-muenster.de
- EICESS-Schema: Chemotherapie + ggf. präoperative Bestrahlung + weite Resektion + ggf. postoperative Bestrahlung + Chemotherapie
- Chemotherapie:
- für die Verbesserung der 5-Jahresüberlebensrate verantwortlich
- first line: Doxorubicin, Methotrexat/Leukovorin, Ifosfamid, Cisplatin
- second line: Carboplatin, Etoposid
- präoperativ: 6 Zyklen induktive neoadjuvante Therapie
- postoperativ: je nach Ansprechen
- Ansprechen nach Salzer & Kuntschik: vitale Tumorzellen im Resektat
- „Good Response“: Grad 1: keine, Grad 2: wenige, Grad 3 <10% vitale Zellen
- „Poor Response“: Grad 4: 10-50%, Grad 5: >50%, Grad 6: komplett vitaler Tumor
- weite en-bloc Resektion: Tumor ist allseits von gesundem Gewebe umgeben (3cm Sicherheitsabstand im Knochen)
- Strahlentherapie: Ewing Sarkome sind strahlensensibel
- präoperativ: bei nicht weit resezierbaren Tumoren
- postoperativ: bei schlechtem Ansprechen des Tumors auf die präoperative Chemotherapie oder bei nicht adäquater Resektion
Prognose / Komplikationen:
- Fünfjahresüberlebensrate
- bei optimaler Therapie (EICESS Protokoll): ca. 60%
- nur Operation und Bestrahlung: ca. 10%
- Risikoparameter: Hochrisikogruppe
- Tumorvolumen >100 ml
- stammnahe Tumorlokalisation
- schlechtere Response auf Chemotherapie nach Salzer & Kuntschik
